Großräumige Strukturen
Die Materie im Universum ist zu einem hohen Grad strukturiert. Die Strukturen sind dabei teilweise so mächtig, dass sie bezüglich der Dynamik des Universums nicht mehr vernachlässigt werden können. Dies passt nicht gut zu den Grundannahmen des Standardmodells (Urknallmodells).
1.0 Inhalt
Die Materie im Universum ist zu einem hohen Grad strukturiert. Diese Strukturen werden schrittweise vorgestellt und ihre Bedeutung für das Verständnis des Universums diskutiert. Die Tatsache, dass es Strukturen bis zu einer Größenordnung von etwa 10 % des Universums gibt, mit dem wir in kausaler Wechselwirkung stehen, widerspricht den Modellannahmen des „Standardmodells“ (https://genesis-net.de/a/1-6/d/4-2/) als eines im großen und ganzen homogenen [= gleichverteil] Universums. Aufgrund der großräumigen Strukturen ergeben sich Abweichungen vom sog. Hubble-Fluss (allgemeine Expansion des Universums).
1.1 Das strukturierte Universum
Im Universum findet man Materie nicht einfach gleichmäßig verteilt. Es sind vielmehr deutlich markante Strukturen ausgeprägt. Das wird bereits deutlich, wenn man einen Blick in unser Sonnensystem wirft. Die Materie ist im Wesentlichen auf wenige Gestirne konzentriert, nämlich vor allem auf die Sonne und dann auf die Planeten und Monde, Planetoiden und Kometen, während der Raum zwischen diesen Körpern praktisch leer ist. Das Sonnensystem ist damit stark strukturiert. Weitet man nun den Blick über das Sonnensystem hinaus, so ändert sich dieses Bild grundsätzlich nicht: Man findet Tausende und Abertausende von diskreten Lichtquellen, die wir als Sterne bezeichnen, während der interstellare [= zwischen den Sternen] Raum wieder praktisch leer ist. Zwar finden sich im interstellaren Raum hin und wieder eindrückliche Gas- und Staubnebel, die generelle Struktur der Materie in Form von Sternen überwiegt aber bei weitem.
1.2 Einleitung
Lässt sich die Strukturiertheit des Universums über die Einheit des Sterns hinaus fortsetzen? Das ist eindeutig der Fall. Beobachtungen haben gezeigt, dass unser Sternsystem die Form einer typischen Spiralgalaxie (Abb. 160) annimmt und damit wiederum zu einer strukturellen Einheit zusammengefasst ist, der Milchstraße. Galaxien (s. https://genesis-net.de/a/1-6/c/3-1/) werden nun seit wenigen Hundert Jahren in großer Zahl und Formenfülle beobachtet, die unser Universum mit ihrer Schönheit bereichern. Jede einzelne von ihnen ist wiederum ein ganzes Sternsystem aus Tausenden und Abertausenden von Sternen wie das unsrige. Galaxien bilden somit die nächste Sprosse der kosmischen „Strukturenleiter“.

Abb. 160: Spiralgalaxie NGC 4414. Quelle: NASA
Nach den bisherigen Ausführungen wird es kaum verwundern, dass sich auch Galaxien zu weiteren Strukturen zusammenfinden: Sie bilden Gruppen oder Haufen. Während eine Gruppe einige wenige bis wenige Dutzend Galaxien enthält, besteht ein Haufen aus einigen Hunderten von Galaxien. Galaxienhaufen zeigen Radio- und Röntgenstrahlung, die aber nicht von einigen diskreten Quellen ausgeht, sondern flächenhaft über den ganzen Haufen verteilt ist. Weiter ergeben Berechnungen zur Dynamik von Galaxienhaufen einen relativ großen Anteil an dunkler Materie, die bisher allerdings nicht nachgewiesen werden konnte (siehe „Dunkle Materie und dunkle Energie“ (https://genesis-net.de/a/1-6/d/4-7/)). Ein Beispiel für eine Galaxien-Gruppe ist unsere Lokale Gruppe, der die Milchstraße angehört. Sie besteht aus ungefähr 28 Galaxien, die durch Abstände von bis zu einigen Millionen Lichtjahren getrennt sind. Unsere nächsten Nachbarn sind die Große- und Kleine Magellanische Wolke, die etwa 150 000 Lichtjahre entfernt sind. Weitere bekannte reiche Haufen sind beispielsweise der Virgo-, Coma- oder Herkules-Haufen (Abb. 165). Zwar gibt es auch Galaxien, die nicht zu einer Gruppe gehören, sogenannte Feld-Galaxien. Die meisten Galaxien gehören aber zu einem größeren „Verband“.

Abb. 165: Jeder Helle Fleck ist eine eigene Galaxie. Die hellen Galaxien im Vordergrund bilden den Herkules-Haufen. Es handelt sich um einen irregulären Haufen, d.h. die Galaxien sind nicht um ein Zentrum angeordnet. Dafür ist er reich an Spiralgalaxien. Quelle: University of Alabama.
Ist mit den Galaxienhaufen die letzte Sprosse der hierarchischen Strukturleiter des Universums erreicht? Die Antwort lautet wiederum nein. Das Studium der Verteilung von Galaxienhaufen im Universum hat die Existenz noch größerer Strukturen ergeben. Sie haben eine typische Größenordnung von etwa 150 Millionen Lichtjahren Durchmesser, während typische Galaxienhaufen etwa 10-mal kleiner sind. Man nennt diese größeren Strukturen Superhaufen. Unsere Lokale Gruppe gehört beispielsweise zu einem Superhaufen, dessen Zentrum der Virgo-Haufen ist. Man spricht darum auch vom Virgo-Superhaufen.
1.3 Großräumige Strukturen
Seit den 1970er und 1980er Jahren wurde es aufgrund der beträchtlichen Verbesserung von Beobachtungstechniken bezüglich extragalaktischer [= außerhalb unserer Milchstraße] Quellen möglich, unter Zuhilfenahme des Hubble-Gesetzes (siehe „Rotverschiebung“ (https://genesis-net.de/a/1-6/d/4-3/)) dreidimensionale Karten der Materieverteilung im Universum zu erstellen. Diese zeigten regelmäßig Inhomogenitäten [= nicht gleichmäßig verteilt] von Materie im Universum. Ein Ausschnitt der bisher umfassendsten Untersuchung ist in Abb. 150 gezeigt.
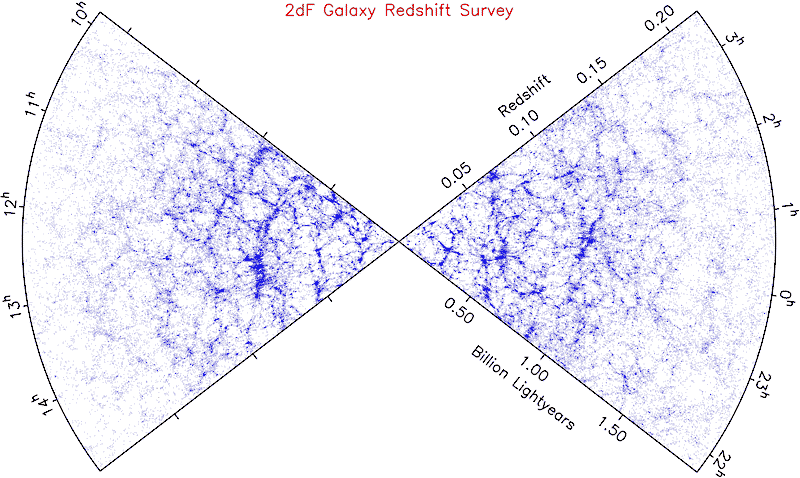
Abb. 150: Ein Auszug aus der 2dF Galaxien Rotverschiebungskarte. Es handelt sich dabei um die detaillierteste Untersuchung überhaupt. In diesem beiden Keilen wurden die Standorte von über 60000 Galaxien abgebildet. Unsere Milchstraße befindet sich genau zwischen den Keilen. Quelle: 2dF Galaxy Redshift Survey Team.
Man findet darin folgende Merkmale:
Superhaufen: Ansammlungen von Galaxien, die eine Größenordnung von einigen Hundert Millionen Lichtjahren umfassen und Tausende von Galaxien enthalten.
Leerräume bis zu einer Größenordnung von über einer halben Milliarde Lichtjahren, in denen sich praktisch keine Galaxien befinden.
Filamente: Die einzelnen Superhaufen sind durch gut sichtbare Filamente [= fadenartige Strukturen] miteinander verbunden.
In den 1920er und 1930er Jahren wurde allgemein angenommen, dass das Universum auf genügend großer Skala homogen [= gleichverteilt] sei. Dies führte zum Postulat des kosmologischen Prinzips, die das Fundament des „Standardmodells“ (https://genesis-net.de/a/1-6/d/4-2/) (Urknallmodells) bildet. Das kosmologische Prinzip besagt, dass das Universum im großen und ganzen homogen [= gleichverteilt ohne Strukturen] und isotrop [= in alle Richtungen gleich] sei. Angesichts dieser neueren Rotverschiebungskarte (Abb. 150, s. o.) wird aber deutlich, dass diese Annahme zu einfach ist. Das Universum ist selbst in Größenordnungen von über einer Halben Milliarde Lichtjahren alles andere als homogen. Das umfasst ungefähr 10 % des Universums, zu dem wir nach dem Standardmodell durch Kausalität [= Ursache und Wirkung] verbunden sind. Damit kann das kosmologische Prinzip nicht mehr als eine erste Näherung an das wirkliche Universum sein. Weiter besteht im Rahmen des Standardmodells das Problem, wie sich diese riesigen Strukturen überhaupt im Kontext eines ausdehnenden Universums bilden konnten. Angesichts des sehr homogenen „Mikrowellenhintergrunds“ (https://genesis-net.de/a/1-6/d/4-5/), der die Materieverteilung in einem frühen Stadium repräsentieren soll, wird das Problem sogar zusätzlich verstärkt. Ohne einen wesentlichen Bestandteil von dunkler Materie (s. „Dunkle Materie und dunkle Energie“ (https://genesis-net.de/a/1-6/d/4-7/)) ist es nicht zu bewältigen.
1.4 Abweichungen vom Hubble-Fluss
Die großräumigen Strukturen des Universums werden zu Abweichungen des sog. Hubble-Flusses führen. Der Hubble-Fluss ist der allgemeine Trend der Galaxien im ausdehnenden Universum und wird durch das Hubble-Gesetz wiedergegeben (siehe „Rotverschiebung“ (https://genesis-net.de/a/1-6/d/4-3/)). Die Abweichungen entstehen durch die starke Gravitationsanziehung großer Massenansammlungen. Unsere Lokale Gruppe weist auch eine Eigenbewegung gegenüber dem extragalaktischen Hintergrund und gegenüber dem „Mikrowellenhintergrund“ (https://genesis-net.de/a/1-6/d/4-5/) auf. Für diese Bewegung wird der Große Attraktor verantwortlich gemacht, auf den wir uns scheinbar zu bewegen. Da sich allerdings in der vermuteten Region des Großen Attraktors keine sichtbaren Massenansammlungen befinden und auch kein Rückeinfall von Galaxienhaufen auf der anderen Seite des Attraktors beobachtet werden konnte, wurden schließlich beträchtliche Zweifel an seiner Existenz geäußert. Dies ist ein Beispiel dafür, wie unvollkommen unser Bild der großräumigen Strukturen und ihrer Dynamik noch immer ist. Die daraus entstehenden Unsicherheiten wirken sich auf die Bestimmung der Hubble-Konstante (siehe „Rotverschiebung“ (https://genesis-net.de/a/1-6/d/4-3/)) aus, die nur den wirklichen Hubble-Fluss erfassen sollte, und erschweren die Interpretation der Rotverschiebungskarten (Abb. 150, s. o.) anhand des Hubble-Gesetzes als räumliche Karten des Universums. Schließlich sollten die Distanzen nur durch den Rotverschiebungsanteil des Hubble-Flusses berechnet werden.
1.5 Kommentar
Ein Universum mit derart ausgeprägten Strukturen wurde von den Kosmologen nicht erwartet. Das Ausmaß der Strukturen umfasst Distanzen von über einer halben Milliarde Lichtjahren. Das widerspricht der Grundannahme des Standardmodells, wonach das Universum im Mittel homogen ist, und erschwert die Modellbildung des Universums. Die großräumigen Strukturen sind zu einer Herausforderung für das Standardmodell geworden, die ohne einen großen Anteil dunkler Materie im Universum nicht zu bewältigen ist. Es ist außerdem möglich, dass die Strukturleiter mit dem heutigen Verständnis der großräumigen Struktur noch gar nicht beendet ist. Entsprechende Behauptungen müssen aber erst bestätigt werden.
Andererseits kann man festhalten, dass die Strukturen einem bewohnbaren Universum grundsätzlich entgegen kommen. Wäre die Materie im Universum praktisch gleichverteilt ohne markante Strukturen, wäre Leben, wie wir es kennen, nicht möglich. Die Strukturen sind aber nicht nur für das Leben förderlich, sondern machen das Universum mit der Vielfalt an Galaxien und anderen Objekten erst schön und interessant.
1.6 Literatur
Narlikar J.V. (2002) An Introduction to Cosmology. Cambridge University Press. Third Edition.
Autor: Studiengemeinschaft Wort und Wissen, 19.09.2004
Aktualisiert am 07.01.2024 (B. Scholl); © beim Autor; alter Link: 2004, https://www.genesisnet.info/schoepfung_evolution/i42462.php